匯玩客App數字內容制作服務產品說明
匯玩客App產品說明PPT設計
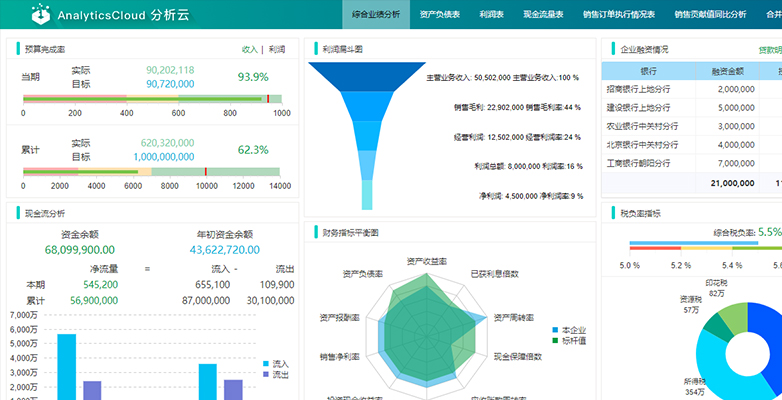
產品核心價值:一站式數字內容制作服務平臺
匯玩客App致力于為用戶提供高效、便捷、專業的數字內容制作服務,幫助個人創作者與企業客戶輕松應對短視頻、圖文、直播等多種內容形式的需求。我們集成了強大的創意工具、豐富的資源庫與智能化的協作流程,讓內容創作從構思到發布變得前所未有的簡單。
核心服務模塊
1. 智能創意與策劃
AI靈感生成器:基于用戶輸入的關鍵詞與目標,智能生成創意腳本、文案大綱與拍攝分鏡建議。
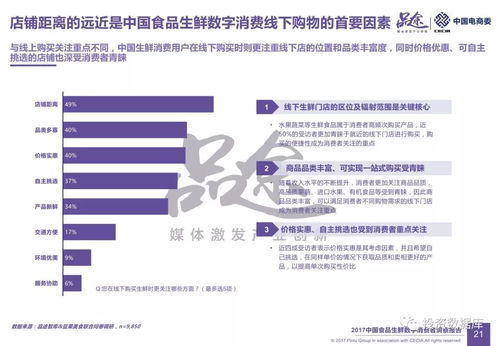
熱點追蹤與選題庫:實時同步全網熱點話題,提供數據化選題分析與趨勢預測,確保內容時效性與吸引力。
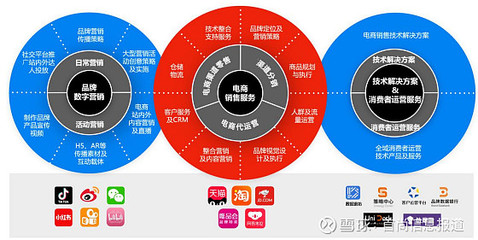
* 定制化內容策劃:針對企業品牌宣傳、產品推廣等需求,提供專業的全案內容策略與規劃服務。
2. 高效內容生產工具集
多格式視頻編輯器:支持橫屏、豎屏、多尺寸剪輯,內置專業級濾鏡、轉場、特效與字幕模板,一鍵應用,大幅提升制作效率。
圖文設計與排版:提供海量可商用模板,涵蓋海報、長圖、信息圖等多種形式,拖拽式操作,輕松完成高質量視覺設計。
* 云端素材管理:集成正版圖片、視頻、音樂、字體庫,支持團隊云端協同管理與調用,保障素材安全與版權合規。
3. 專業直播解決方案
多平臺推流與管理:支持一鍵同步開播至主流視頻與社交平臺,并集中管理直播數據與互動。
虛擬場景與互動工具:提供豐富的虛擬背景、貼紙、禮物特效及互動組件(如抽獎、投票),增強直播趣味性與觀眾參與感。
* 直播數據復盤:生成多維度的直播數據分析報告,助力優化直播策略與提升轉化效果。
4. 全流程協作與項目管理
團隊任務看板:清晰分配內容策劃、拍攝、剪輯、審核等任務,實時同步進度,確保項目按時交付。
在線審閱與批注:支持團隊成員在線對內容進行標記、評論與修改,版本歷史清晰可追溯,溝通效率倍增。
* 資產管理與企業服務:為企業客戶提供專屬內容資產庫、品牌視覺規范管理及VIP客戶成功經理支持。
技術優勢與安全保障
- 云端智能渲染:復雜特效與高清導出無需消耗本地算力,通過云端集群快速完成。
- 數據驅動優化:基于用戶行為與內容表現數據,智能推薦優化方向與模板,助力內容效果提升。
- 企業級安全與隱私:數據加密傳輸與存儲,嚴格的權限管理機制,確保商業內容與數據的絕對安全。
目標用戶群體
- 內容創作者與自媒體人:尋求提升內容質量與生產效率的個人或團隊。
- 中小企業市場與運營部門:需要持續產出高質量營銷內容,但缺乏專業設計與視頻團隊的品牌。
- 電商商家與直播主播:需要制作產品介紹、活動促銷視頻及進行常態化直播的賣家與達人。
- 企業培訓與內部通訊部門:需要制作培訓課程、企業文化宣傳視頻等內部內容的組織。
為何選擇匯玩客?
- All-in-One集成平臺:告別在多款軟件間切換的繁瑣,一個平臺滿足從策劃到發布的全鏈條需求。
- 技術降低專業門檻:將復雜的專業制作流程簡化為直觀的操作,讓非專業人士也能產出專業級內容。
- 成本效益顯著:相比組建或外包專業團隊,以極低的訂閱成本即可獲得持續、穩定的高質量內容產出能力。
- 持續進化與支持:產品基于用戶反饋與市場趨勢快速迭代,并提供7x24小時的在線客服與豐富的教程資源。
匯玩客App,不僅是工具,更是您數字內容創作路上的得力伙伴與增長引擎。即刻開啟,釋放無限創意!
最新產品